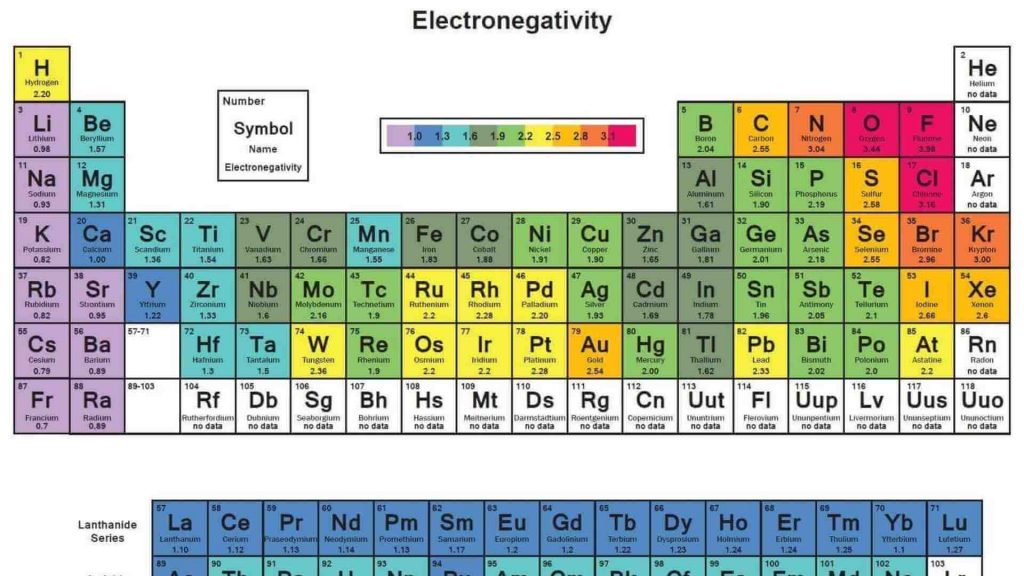
Elettronegatività: come calcolarla in pochi passaggi
In chimica, l‘elettronegatività è la misura della quantità di forza con cui un atomo attrae gli elettroni in un legame. Un atomo con un’elevata elettronegatività attrae elettroni con grande forza, mentre uno con una bassa elettronegatività li attrae debolmente.
I valori dell’elettronegatività servono a prevedere come si comportano i diversi atomi quando si uniscono tra loro, il che rende questa grandezza molto importante nella chimica di base.
Che cos’è un collegamento tra atomi?
Per comprendere meglio il concetto di elettronegatività, è importante prima capire che cos’è un collegamento tra atomi. Si dice che due atomi sono collegati l’uno all’altro in un diagramma molecolare; ciò significa che condividono un insieme di due elettroni in cui ogni atomo porta un elettrone al legame.
Quando due atomi condividono un insieme di due elettroni in un legame, non sempre lo fanno allo stesso modo. Quando un atomo ha una maggiore elettronegatività di quella a cui è legato, attirerà i due elettroni a se stesso. Ad esempio, nella molecola di NaCl (cloruro di sodio), l’atomo di cloro ha un’elettronegatività molto elevata e il sodio ha un valore piuttosto basso; pertanto, gli elettroni saranno attratti dal cloruro piuttosto che dal sodio.
Il metodo di Mulliken: come calcolare l’elettronegatività
Quello di Mulliken è un metodo leggermente diverso di calcolare l’elettronegatività rispetto a quello utilizzato nella tabella di Pauling. Dunque, per ricavare l’elettronegatività di un atomo, bisogna trovare la prima energia di ionizzazione di quell’atomo.
Ad esempio, supponiamo di dover calcolare l’elettronegatività del litio (Li).
Nella tabella degli elementi, possiamo vedere che la sua prima energia di ionizzazione è di 520 kJ / mol.
A questo punto dobbiamo trovare l’affinità elettronica dell’atomo. Questa è la misura dell’energia ottenuta quando un elettrone viene aggiunto a un atomo per formare uno ione negativo. L’affinità elettronica del litio è di 60 kJ mol -1.
Risolvere l’equazione di Mulliken
Quando si usa kJ / mol come unità per le energie, l’equazione di Mulliken sarà: M= (1.97 × 10 -3) (E i + E bis) + 0.19 . Quindi, dobbiamo sostituire i valori nell’equazione e risolverla. Nel nostro esempio, lo risolveremo nel modo seguente: (1.97 × 10 -3) (E i + E bis) + 0.19;
quindi: (1.97 × 10 -3) (520 + 60) + 0.19;
di conseguenza: 1,143 + 0,19 = 1,333.
Nel nostro esempio, dunque, il valore dell’elettronegatività del litio è pari a 1,333.
Oltre ai metodi di Pauling e Mulliken, ci sono anche altre scale di elettronegatività, come quella di Allred-Rochow, la scala Sanderson e la scala Allen. Tutti hanno le loro rispettive equazioni per il calcolo dell’elettronegatività, alcune delle quali possono essere molto complesse. E’ da notare, infine, che l’elettronegatività non ha unità di misura.